最新の薬剤師転職・求人・募集サイトを、口コミ&評判つきで比較・ランキングします。

トップページ > コラム:病院における薬剤師の役割「副作用・感染症報告制度」
薬剤師は景気の好不調の波を受けにくい人気の業種です。しかし、人生の多くの時間を費やすわけですから、やはり、よりよい処遇・よりよい人間関係・よりよい職場環境を求めたいものです。一度しかない人生です。ユーザーのみなさまが、ぜひ素敵な仕事・職場にめぐり合えることを祈っております。
コラム:病院における薬剤師の役割「副作用・感染症報告制度」
製造販売後の制度としては、「再審査制度と安全性定期報告」、「再評価制度」と「副作用・感染症報告制度」があります。
6.副作用・感染症報告制度
この制度の一部については、先の「医薬関係者からの副作用報告制度(医薬品・医療機器等安全性情報報告制度)」の項で記しましたが、この制度はそれ以外に「企業報告制度」、「感染症定期報告制度(生物由来製品)」と「WHO国際医薬品モニタリング制度」からなります。
「企業報告制度」は、薬事法により製薬企業に課せられた義務で、これを怠ると行政処分を受けるものです。
「感染症定期報告制度(生物由来製品)」は、人や動物に由来する原料で製造される生物由来製品について特別に行われるものです。
「WHO国際医薬品モニタリング制度」は、国際的な副作用情報の情報交換を行う制度であり、我が国は1972年から参加しています。下図に副作用報告制度の概略を示しました。
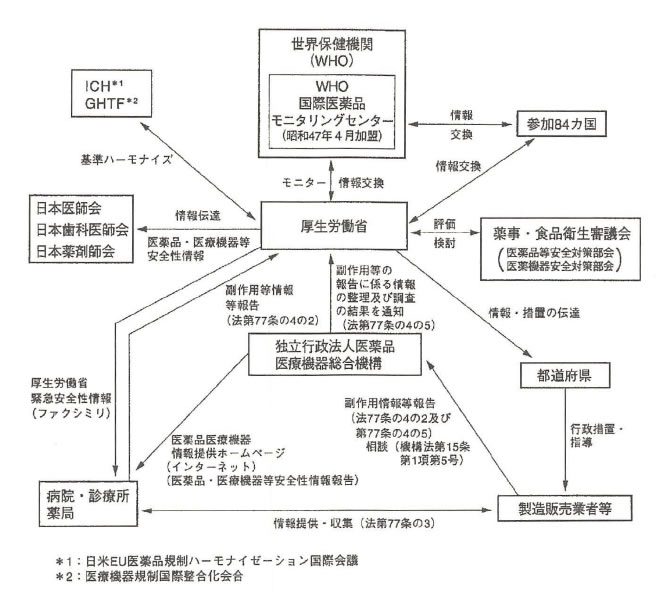
参考になさってください。
>>>今月の薬剤師転職サイト比較/口コミ人気ランキングはこちら
病院における薬剤師の役割
- トップページ
- 薬剤師/転職・求人サイト比較
- 病院における薬剤師の役割
-
- 病院の薬剤師
- 病院薬剤師の業務
- 病院薬剤師の調剤業務
- 病院薬剤師の薬剤管理指導業務
- 病院薬剤師の製剤業務
- 病院薬剤師の薬品管理業務
- 病院薬剤師の医薬品情報管理業務
- 病院薬剤師の薬品試験業務
- 病院薬剤師の治験業務
- これからの病院薬剤師
- 病院数の推移
- 薬剤師数の推移
- DPC対象病院と包括払い
- 病院の収支構造
- 病院の収入になる要素
- 病院の支出される内容
- 病院薬剤師が関与する保険点数(診療報酬)
- 持参薬の活用
- 地域医療
- 薬薬連携
- 医薬分業の基本的なスタンスと考え方
- 医師が薬を必要以上に多く出す理由
- 政策誘導、利益誘導を力に進められた医薬分業
- 病院薬剤師の新たな取り組み
- 医薬分業の問題点
- 門前薬局の問題点と解決策
- 世界の薬剤師の動向
- 我が国における医療改革
- 薬剤師と包括医療
- 薬学教育6年制が決定された背景
- 6年制の薬学教育の目的
- 医療現場での薬剤師の3つの機能
- 育薬とは
- 我が国の新薬発売後の問題点
- 育薬の実際(ランソプラゾールを例に)
- 医薬関係者からの副作用報告制度
- 医療機関における医薬情報(DI)活動
- 医薬品の再審査制度
- 医薬品の製造販売後の調査および試験の実施の基準
- 安全性定期報告
- 医薬品の製造販売後安全管理の基準(GVP省令)
- 医薬品の再評価制度
- 副作用・感染症報告制度
- 医薬品副作用被害救済制度
相互リンク
目次
- トップページ
- 薬剤師/転職・求人サイト比較
-
- エムスリーキャリア(m3キャリア)「薬キャリ(m3.comファーマシスト)」の口コミ・評判
- マイナビ「マイナビ薬剤師」の口コミ・評判
- ディップ「薬剤師ではたらこ」の口コミ・評判
- リクルートドクターズキャリア「リクナビ薬剤師」の口コミ・評判
- メディカルリソース「ファルマスタッフ」の口コミ・評判
- メディカル・コンシェルジュ「MC−ファーマネット」の口コミ・評判
- レバレジーズ「薬剤師のお仕事」の口コミ・評判
- →突撃インタビュー「薬剤師のお仕事」
- メディプロ「ゴリ薬(薬剤師プロ!)」の口コミ・評判
- ユニヴ「ファーネットキャリア」の口コミ・評判
- インテリジェンス「DODA薬剤師」の口コミ・評判
- キャリアブレイン「CBネット」の口コミ・評判
- グローアップ「薬剤師ステーション(ヤクステ)」の口コミ・評判
- メディウェル「薬剤師転職ドットコム」の口コミ・評判
- プロト「薬剤師求人エージェント」の口コミ・評判
- 生き残る薬剤師とは?
- 丸分かり!薬剤師
-
- 丸分かり!薬剤師1「薬剤師とは」
- 丸分かり!薬剤師2「薬剤師になるには」
- 丸分かり!薬剤師3「薬剤師国家試験の概要と合格率」
- 丸分かり!薬剤師4「薬剤師の就職状況」
- 丸分かり!薬剤師5「薬剤師の1日はどんな感じ?」
- 丸分かり!薬剤師6「薬剤師の歴史、起源」
- 丸分かり!薬剤師7「薬剤師の調剤業務の中身は?」
- 丸分かり!薬剤師8「薬剤師の調剤以外のお仕事は?」
- 丸分かり!薬剤師9「薬剤師の仕事場はどこ?」
- 丸分かり!薬剤師10「薬剤師の生活と収入」
- 丸分かり!薬剤師11「薬剤師になる手順」
- 丸分かり!薬剤師12「薬剤師向きな人、不向きな人」
- 丸分かり!薬剤師13「薬剤師の将来」
- 丸分かり!薬剤師14「薬に関する基礎知識」
- 丸分かり!薬剤師15「薬局とは?」
- 丸分かり!薬剤師16「医薬品販売業とは?」
- 丸分かり!薬剤師17「薬剤師に関係する法律は?」
- 丸分かり!薬剤師18「薬剤師に求められる役割は?」
- 丸分かり!薬剤師19「かかりつけ薬剤師という役割」
- 丸分かり!薬剤師20「薬剤師の仕事〜処方箋の受付」
- 丸分かり!薬剤師21「薬剤師の仕事〜薬暦管理」
- 丸分かり!薬剤師22「薬剤師の仕事〜服薬指導」
- 丸分かり!薬剤師23「薬剤師の仕事〜保険点数計算」
- 薬剤師の転職に関するアドバイス
-
- アドバイス1「薬剤師の転職は簡単ですか?」
- アドバイス2「薬剤師の転職で年齢は重要ですか?」
- アドバイス3「薬剤師の転職のコツは何ですか?」
- アドバイス4「薬剤師の転職で昇給できますか?」
- アドバイス5「薬剤師の転職で高収入を狙えますか?」
- アドバイス6「薬剤師の転職の流れを教えてください。」
- アドバイス7「薬剤師の転職で、良い職場を探すポイントを教えてください。」
- アドバイス8「ペーパー薬剤師の転職で、不安です。」
- アドバイス9「薬剤師転職支援会社の上手な利用方法は?」
- アドバイス10「薬剤師の転職は出世に不利ですか?」
- アドバイス11「薬剤師の転職後の年収相場を教えてください。」
- アドバイス12「薬剤師の転職先として、業態別の長所・短所を教えてください。」
- アドバイス13「薬剤師の転職情報はどこで探せばよいですか?」
- アドバイス14「チェーン店の調剤薬局に転職する際の注意点を教えてください。」
- アドバイス15「転職先として、薬局チェーン大手と個人経営の薬局、どちらがいいでしょうか?」
- アドバイス16「病院薬剤師への転職は難しいですか?」
- アドバイス17「公務員薬剤師への転職とお仕事は?」
- アドバイス18「病院から調剤薬剤師への転職はどうですか?」
- 薬剤師に関する基礎知識
- 病院における薬剤師の役割
-
- 病院の薬剤師
- 病院薬剤師の業務
- 病院薬剤師の調剤業務
- 病院薬剤師の薬剤管理指導業務
- 病院薬剤師の製剤業務
- 病院薬剤師の薬品管理業務
- 病院薬剤師の医薬品情報管理業務
- 病院薬剤師の薬品試験業務
- 病院薬剤師の治験業務
- これからの病院薬剤師
- 病院数の推移
- 薬剤師数の推移
- DPC対象病院と包括払い
- 病院の収支構造
- 病院の収入になる要素
- 病院の支出される内容
- 病院薬剤師が関与する保険点数(診療報酬)
- 持参薬の活用
- 地域医療
- 薬薬連携
- 医薬分業の基本的なスタンスと考え方
- 医師が薬を必要以上に多く出す理由
- 政策誘導、利益誘導を力に進められた医薬分業
- 病院薬剤師の新たな取り組み
- 医薬分業の問題点
- 門前薬局の問題点と解決策
- 世界の薬剤師の動向
- 我が国における医療改革
- 薬剤師と包括医療
- 薬学教育6年制が決定された背景
- 6年制の薬学教育の目的
- 医療現場での薬剤師の3つの機能
- 育薬とは
- 我が国の新薬発売後の問題点
- 育薬の実際(ランソプラゾールを例に)
- 医薬関係者からの副作用報告制度
- 医療機関における医薬情報(DI)活動
- 医薬品の再審査制度
- 医薬品の製造販売後の調査および試験の実施の基準
- 安全性定期報告
- 医薬品の製造販売後安全管理の基準(GVP省令)
- 医薬品の再評価制度
- 副作用・感染症報告制度
- 医薬品副作用被害救済制度
- 薬剤師とセルフメディケーション
-
- 衣食住から医・衣・食・住へ
- セルフメディケーションと国民皆保険制度
- 社会保障の財政危機と対応
- セルフメディケーションの定義
- セルフメディケーションの効用
- セルフメディケーション実践へのステップ
- 地域を基盤とするセルフメディケーション体制
- セルフメディケーションを支援する人材
- セルフメディケーションにおける薬剤師の役割
- セルフメディケーションと薬学教育の変遷
- 薬剤師職能のコペルニクス的転換
- 在宅療養での薬剤師の役割
- 在宅療養の制定
- 薬剤師が行う居宅療養管理指導
- 在宅療養へのシフト
- 居宅療養管理指導の推移
- 入院療養から居宅療養への移行
- クリニカルパスと薬剤師
- 居宅療養の現場
- ゲシュタルトの法則による在宅指導
- 在宅療養は避けて通れない
- 薬剤師と地域医療
- 薬剤師を取り巻く環境
-
- 再編・淘汰が進む調剤薬局
- 調剤薬局の商圏が変わる
- 調剤偏重からの脱却が必要
- 門前薬局の終焉の始まり
- 突合点検、縦覧点検とは
- 電子レセプトとは
- 突合点検・縦覧転換の影響
- 査定分の取り扱い
- 医薬分業では情報交換が大切
- 集団指導、個別指導、監査
- 薬剤師の売り手市場はいつまで?
- 薬局数が減っていく理由
- 代替わりの時期を迎えた薬局
- ドラッグストアの歴史
- ドラッグストアの今後の課題
- 薬剤師の大量採用は一過性?
- 医薬分業と薬剤師の問題点
- 現状の医薬分業体制への危機感
- 事業仕分けで調剤不正が問題に
- 薬歴管理算定もノーチェック
- 調剤手順変更の真意
- 総人口減少でも高齢者は増加
- 在宅患者ニーズを掘り起こせ
- 割に合わない薬剤師の在宅訪問
- 在宅訪問に薬剤師のPRが必要
- 在宅現場での薬剤師の役割
- ドラッグストア、調剤参入の狙い
- 調剤薬局は面展開・新業態で対抗
- 調剤助手導入で薬剤師は半減?
- ドラッグストア薬剤師の現状
- 調剤薬局は地域連携が鍵
- 薬局とドラッグストアの土俵
- 地場薬局の未来
- 薬剤師関連ニュース

